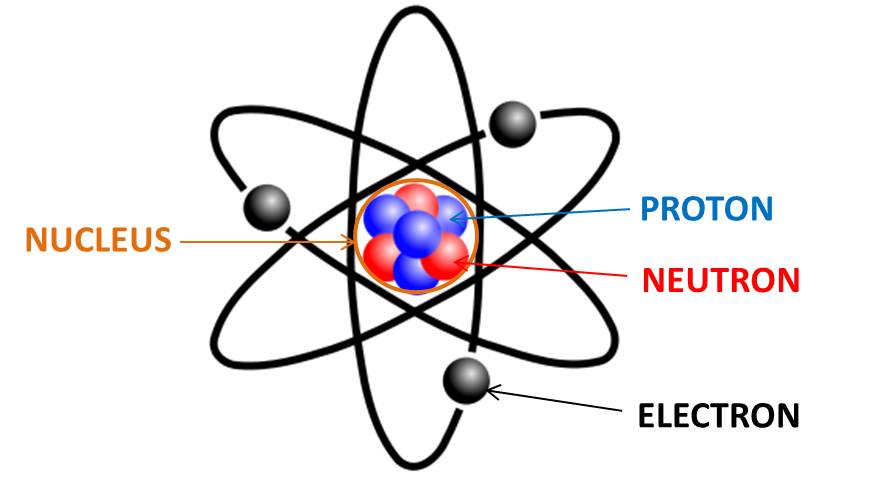
Apa Itu Atom?
Atom adalah unit terkecil dari suatu unsur kimia yang masih mempertahankan sifat dan identitas kimia unsur tersebut. Atom terdiri dari inti atom yang mengandung partikel subatomik yang disebut proton dan neutron, serta elektron yang mengorbit mengelilingi inti atom. Atom terdiri dari proton, yang memiliki muatan positif, dan neutron, yang tidak memiliki muatan. Jumlah proton dalam inti atom menentukan identitas unsur kimia tersebut.
Misalnya, atom dengan satu proton adalah atom hidrogen, sedangkan atom dengan enam proton adalah atom karbon. Elektron adalah partikel yang mengorbit di sekitar inti atom dalam orbit yang ditentukan. Elektron memiliki muatan negatif yang seimbang dengan muatan positif proton di inti atom. Jumlah elektron dalam suatu atom dapat berbeda-beda, tetapi atom secara umum memiliki jumlah elektron yang sama dengan jumlah proton, sehingga atom bersifat netral secara muatan.
Sejarah Atom
Sejarah atom bermula pada zaman kuno dengan gagasan-gagasan filosofis mengenai alam semesta dan materi. Namun, perkembangan yang lebih signifikan dalam pemahaman tentang atom dimulai pada abad ke-19 dan berlanjut hingga abad ke-20. Berikut adalah ringkasan dari perkembangan sejarah atom:
- Filosofi Kuno:
Leukippos dan Demokritos (abad ke-5 SM) mengajukan gagasan tentang atom sebagai partikel-partikel tak terbagi yang membentuk materi. - Model Dalton:
Pada tahun 1803, John Dalton mengajukan model atom pertama yang berdasarkan pada ide atom sebagai partikel indivisible yang memiliki berat dan reaktivitas yang berbeda. - Penemuan Partikel Subatomik:
Pada akhir abad ke-19, eksperimen yang dilakukan oleh J.J. Thomson menemukan adanya partikel bermuatan negatif yang disebut elektron, yang menunjukkan bahwa atom bukanlah partikel tak terbagi. Ia mengajukan model roti kismis untuk atom. - Model Rutherford:
Pada tahun 1911, Ernest Rutherford melakukan percobaan hamburan partikel alfa dan menemukan bahwa atom terdiri dari inti kecil yang bermuatan positif yang disebut inti atom, dengan sebagian besar ruang atom kosong. Elektron mengorbit di sekitar inti atom. Model ini dikenal sebagai model atom Rutherford. - Model Bohr:
Pada tahun 1913, Niels Bohr mengusulkan model atom yang lebih maju. Model Bohr menunjukkan bahwa elektron mengorbit di sekitar inti atom dalam orbit diskrit dengan tingkat energi tertentu. Model ini membantu menjelaskan spektrum atom hidrogen dan konsep tingkat energi atom. - Teori Kuantum:
Pada tahun 1920-an, perkembangan mekanika kuantum oleh fisikawan seperti Werner Heisenberg dan Erwin Schrödinger memberikan pemahaman yang lebih mendalam tentang perilaku partikel subatomik. Teori kuantum menjelaskan sifat gelombang partikel dan memperkenalkan konsep orbital sebagai daerah probabilitas yang menentukan keberadaan elektron dalam atom. - Model Atom Modern:
Model atom modern yang paling diterima adalah model atom kuantum, yang menggabungkan konsep mekanika kuantum dengan teori atom yang lebih lama. Model ini menjelaskan struktur atom dan perilaku partikel subatomik dengan tingkat akurasi yang tinggi.
Struktur Atom
Struktur atom mengacu pada organisasi dan komponen utama yang membentuk suatu atom. Berikut adalah komponen utama dan struktur atom:
Inti Atom
Inti atom terletak di pusat atom dan mengandung dua partikel subatomik: proton dan neutron.
- Proton: Partikel bermuatan positif yang memberikan identitas unsur atom. Jumlah proton dalam inti atom menentukan nomor atom suatu unsur.
- Neutron: Partikel tanpa muatan (netral) yang juga terdapat dalam inti atom. Neutron memberikan massa atom tetapi tidak mempengaruhi muatan listrik atom.
Elektron
Elektron adalah partikel yang bergerak mengelilingi inti atom dalam orbit yang ditentukan. Elektron memiliki muatan negatif dan mempengaruhi sifat kimia atom.
- Elektron terdistribusi dalam berbagai tingkat energi atau kulit elektron. Kulit elektron terdekat dengan inti memiliki energi lebih rendah dan yang terjauh memiliki energi lebih tinggi.
Kulit Elektron
Kulit elektron adalah daerah di sekitar inti atom tempat elektron mengorbit. Setiap kulit memiliki kapasitas maksimum elektron yang dapat diisi.
- Kulit pertama (K) dapat menampung hingga 2 elektron.
- Kulit kedua (L) dapat menampung hingga 8 elektron.
- Kulit ketiga (M) dapat menampung hingga 18 elektron.
- Pada kulit berikutnya, pola pengisian elektron menjadi lebih kompleks.
Orbit dan Subkulit:
Kulit elektron terbagi menjadi orbit dan subkulit, yang menentukan distribusi elektron dalam atom.
- Orbit (n): Menunjukkan tingkat energi atau jarak relatif dari inti atom. Orbit pertama (n = 1) terdekat dengan inti dan seterusnya.
- Subkulit: Merupakan wilayah dalam suatu orbit di mana elektron ditemukan. Subkulit ditandai dengan huruf (s, p, d, f) dan memiliki jumlah orbital yang berbeda:
-Subkulit s memiliki 1 orbital dan dapat menampung maksimal 2 elektron.
-Subkulit p memiliki 3 orbital dan dapat menampung maksimal 6 elektron.
-Subkulit d memiliki 5 orbital dan dapat menampung maksimal 10 elektron.
-Subkulit f memiliki 7 orbital dan dapat menampung maksimal 14 elektron.
Konfigurasi Elektron:
Konfigurasi elektron menggambarkan cara di mana elektron terisi dalam kulit, orbit, dan subkulit atom. Konfigurasi ini mengikuti prinsip-prinsip seperti aturan Aufbau, aturan Hund, dan aturan eksklusi Pauli.